Circuitos Moleculares Compartidos entre las Células Placentales y las Células Tumorales
-
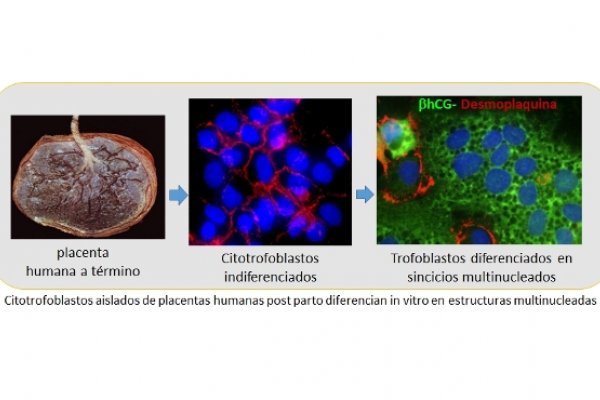 Circuitos Moleculares Compartidos entre las Células Placentales y las Células Tumorales
Circuitos Moleculares Compartidos entre las Células Placentales y las Células Tumorales
-
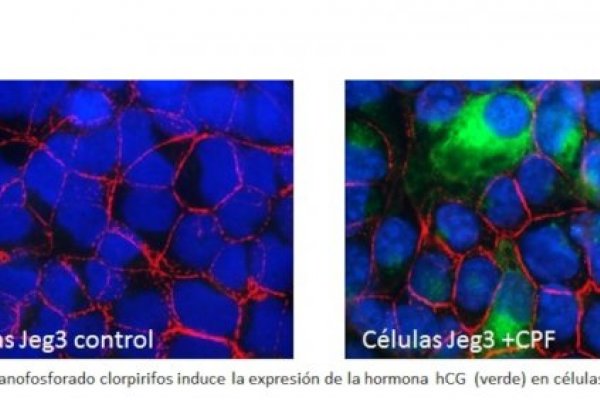 Circuitos Moleculares Compartidos entre las Células Placentales y las Células Tumorales
Circuitos Moleculares Compartidos entre las Células Placentales y las Células Tumorales
-
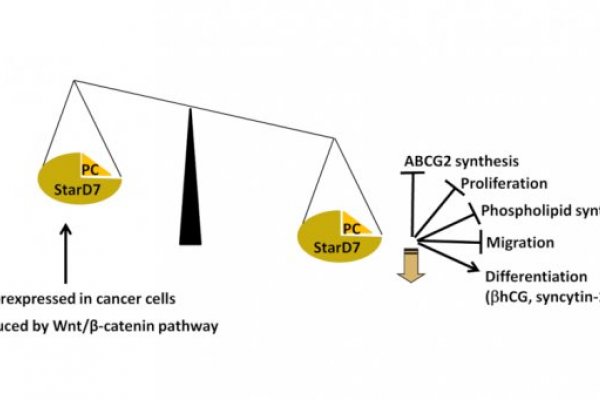 Circuitos Moleculares Compartidos entre las Células Placentales y las Células Tumorales
Circuitos Moleculares Compartidos entre las Células Placentales y las Células Tumorales